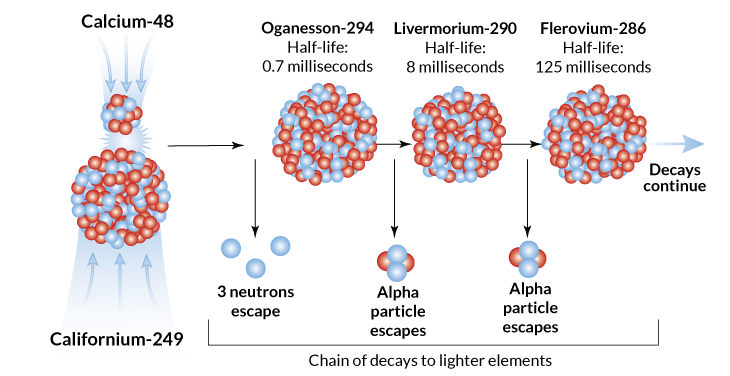A rara substância radioactiva viajou dos Estados Unidos para a Rússia em um voo comercial em Junho de 2009. Os funcionários da alfândega se recusaram a aceitar o pacote, que estava protegido por uma protecção de chumbo e estampado com advertências em negrito e os sinistros símbolos do trevo para radiação ionizante. . De volta, atravessou o Atlântico.
Cientistas norte-americanos anexaram documentação adicional e o pacote fez uma segunda viagem, apenas para ser rejeitado novamente. Enquanto isso, a carga preciosa, 22 miligramas de um elemento chamado berquélio, criado num reator nuclear no Laboratório Nacional de Oak Ridge, no Tennessee, deteriorava-se. Dia após dia, seus átomos decaíam. “Estávamos todos um pouco frenéticos”, diz Julie Ezold, engenheira nuclear de Oak Ridge.
Na terceira tentativa, a remessa passou pela alfândega. Num laboratório em Dubna, a norte de Moscovo, os cientistas misturaram o berquélio com iões de cálcio para tentar criar uma substância ainda mais rara. Após 150 dias de ataques, os pesquisadores detectaram seis átomos de um elemento que nunca havia sido visto na Terra. Em 2015, após outros experimentos confirmarem a descoberta, o elemento 117, tennessine, ganhou um lugar na tabela periódica ( SN: 6/02/16, p. 7 ).

Os cientistas esperam ampliar ainda mais a tabela periódica, além do tennessine e de três outros elementos recentemente descobertos (113, 115 e 118) que completaram a sétima linha da tabela. A produção dos próximos elementos exigirá o aperfeiçoamento de novas técnicas usando feixes ultrapoderosos de íons, átomos eletricamente carregados. Sem mencionar o stress de transportar mais material radioactivo através das fronteiras.
Mas as questões que circulam em torno dos limites da tabela periódica são demasiado tentadoras para não fazermos esse esforço. Já se passaram 150 anos desde que o químico russo Dmitrii Mendeleev criou sua tabela periódica. No entanto, “ainda não conseguimos responder à pergunta: Qual é o elemento mais pesado que pode existir?” diz o químico nuclear Christoph Düllmann, do Centro GSI Helmholtz para Pesquisa de Íons Pesados, em Darmstadt, Alemanha.
No extremo da tabela periódica, os elementos decaem instantes após a sua formação, oferecendo muito pouco tempo para estudar as suas propriedades. Na verdade, os cientistas ainda sabem pouco sobre o mais recente grupo de elementos recém-descobertos. Assim, enquanto alguns cientistas procuram elementos nunca antes vistos, outros querem aprender mais sobre os recém-chegados à mesa e os comportamentos estranhos que esses elementos superpesados podem apresentar.
Para átomos tão grandes, a química pode ficar estranha, pois os núcleos atômicos, os corações no centro de cada átomo, estão repletos de centenas de prótons e nêutrons. Ao redor deles giram grandes bandos de elétrons, alguns se movendo próximo à velocidade da luz. Tais condições extremas podem ter grandes consequências – bagunçar a ordem organizada da tabela periódica, na qual os elementos de cada coluna são parentes químicos próximos que se comportam de maneira semelhante.

Os cientistas continuam a avançar ainda mais com estes elementos superpesados como parte da busca pelo que é poeticamente conhecido como a ilha da estabilidade. Espera-se que os átomos com certo número de prótons e nêutrons vivam mais do que seus amigos fugazes, persistindo talvez por horas, em vez de frações de segundo. Tal ilha daria aos cientistas tempo suficiente para estudar esses elementos mais de perto e compreender as suas peculiaridades. Os primeiros vislumbres desse atol misterioso foram avistados, mas não está claro como conseguir uma posição firme em suas costas.
Por trás de todo esse esforço está uma profunda curiosidade sobre como os elementos agem nos limites da tabela periódica. “Isso pode parecer piegas, mas na verdade trata-se apenas de pura compreensão científica”, diz a química nuclear Dawn Shaughnessy, do Laboratório Nacional Lawrence Livermore, na Califórnia. “Temos essas coisas que estão realmente nos extremos da matéria e não entendemos agora como elas se comportam.”
Mas para produzir os elementos mais pesados, os investigadores adotaram uma nova abordagem de força bruta: lançar feixes de átomos pesados num alvo, um disco que contém átomos de outro elemento. Se os cientistas tiverem sorte, os átomos no feixe e no alvo fundem-se, criando um novo átomo com um núcleo maior e mais volumoso, talvez contendo mais protões do que qualquer outro conhecido.
Os pesquisadores estão usando essa estratégia para ir atrás dos elementos 119 e 120. Os cientistas querem criar esses átomos nunca antes vistos para testar até onde vai a tabela periódica, para satisfazer a curiosidade sobre as forças que mantêm os átomos juntos e para entender o que a química bizarra pode causar. ocorrem com esses átomos extremos.
A persuasão de núcleos para se combinarem em um novo elemento é feita apenas em instalações altamente especializadas em alguns locais do mundo, incluindo laboratórios na Rússia e no Japão. Os pesquisadores escolhem cuidadosamente a composição do feixe e do alvo na esperança de produzir um átomo de design do elemento desejado. Foi assim que os quatro elementos mais novos foram criados : nihonium (elemento 113), moscovium (115), tennessine (117) e oganesson (118) ( SN Online: 30/11/16 ).
Para criar a tennessina, por exemplo, os cientistas combinaram feixes de cálcio com um alvo feito de berquélio – uma vez que o berquélio finalmente conseguiu passar pela alfândega na Rússia. A união faz sentido quando se considera o número de prótons em cada núcleo. O cálcio tem 20 prótons e o berquélio tem 97, perfazendo um total de 117 prótons, número encontrado no núcleo do tennessine. Combine o cálcio com o próximo elemento da tabela, californium, e você obterá o elemento 118, oganesson.
O uso de feixes de cálcio – especificamente um isótopo de cálcio estável com um total combinado de 48 prótons e nêutrons conhecido como cálcio-48 – tem sido altamente bem-sucedido. Mas para criar núcleos maiores seriam necessários materiais cada vez mais exóticos. O califórnio e o berquélio utilizados em esforços anteriores são tão raros que os materiais alvo tiveram de ser fabricados em Oak Ridge, onde os investigadores cozinham materiais num reactor nuclear durante meses e processam cuidadosamente o produto altamente radioactivo que sai. Todo esse trabalho pode produzir apenas miligramas do material.
Para descobrir o elemento 119 usando um feixe de cálcio-48, os pesquisadores precisariam de um alvo feito de einstênio (elemento 99), que é ainda mais raro que o califórnio e o berquélio. “Não conseguimos produzir einstênio suficiente”, diz James Roberto, físico de Oak Ridge. Os cientistas precisam de uma nova abordagem. Eles mudaram para técnicas relativamente não testadas, baseadas em diferentes feixes de partículas.
Mas qualquer nova abordagem teria de produzir novos elementos com frequência suficiente para valer a pena. Demorou quase nove anos para que um experimento japonês provasse a existência do niônio. Naquela época, os pesquisadores detectaram o elemento apenas três vezes.
Para evitar esperas tão longas, os cientistas estão escolhendo cuidadosamente suas táticas e acelerando máquinas melhoradas para acelerar a busca.
Uma equipe do Centro RIKEN Nishina para Ciência Baseada em Aceleradores, perto de Tóquio, usa feixes de vanádio (elemento 23), em vez de cálcio, transformando-os em cúrio (elemento 96) na busca para obter a glória elemental e encontrar o elemento 119. O grupo está começando com um acelerador existente e em breve mudará para um acelerador atualizado para bombear feixes de íons com mais força. Esse acelerador renovado poderá ficar pronto dentro de um ano, diz o químico nuclear da RIKEN, Hiromitsu Haba.
Entretanto, um novo laboratório no Instituto Conjunto de Investigação Nuclear, ou JINR, em Dubna, chamado Superheavy Element Factory, ostenta um acelerador que irá gerar feixes de iões que atingirão o alvo a uma velocidade 10 vezes superior à do seu antecessor. Numa próxima experiência, os cientistas planeiam lançar feixes de titânio (elemento 22) em alvos de berquélio e califórnio para tentar produzir os elementos 119 e 120.
Assim que a nova experiência do JINR estiver em funcionamento, 119 poderá ser descoberto após alguns anos, diz o físico nuclear do JINR, Yuri Oganessian, que deu nome ao oganesson, um dos vários elementos lá descobertos.

Regras da relatividade
A simples detecção de um elemento, entretanto, não significa que os cientistas saibam muito sobre ele. “Como se comportaria um quilograma de fleróvio, se eu o tivesse?” Düllmann pergunta, referindo-se ao elemento 114. “Seria diferente de qualquer outro material.”
Os elementos superpesados conhecidos – aqueles além do número 103 na mesa – têm vida muito curta para criar um pedaço grande o suficiente para segurar na palma da sua mão. Assim, os cientistas limitam-se a estudar átomos individuais, conhecendo cada novo elemento através da análise das suas propriedades, incluindo a facilidade com que reage com outras substâncias.
Uma grande questão é se a periodicidade que dá nome à tabela se aplica a elementos superpesados. Na tabela, os elementos são ordenados de acordo com o número de prótons, dispostos de forma que os elementos de cada coluna tenham propriedades semelhantes. Lítio, sódio e outros da primeira coluna reagem violentamente com água, por exemplo. Os elementos da última coluna, conhecidos como gases nobres, são notoriamente inertes ( SN: 19/01/19, p. 18 ). Mas para os elementos mais novos e mais pesados nos confins da tabela periódica, essa regra de longa data da química pode ser desvendada; alguns elementos superpesados podem se comportar de maneira diferente dos vizinhos sentados acima deles na mesa.
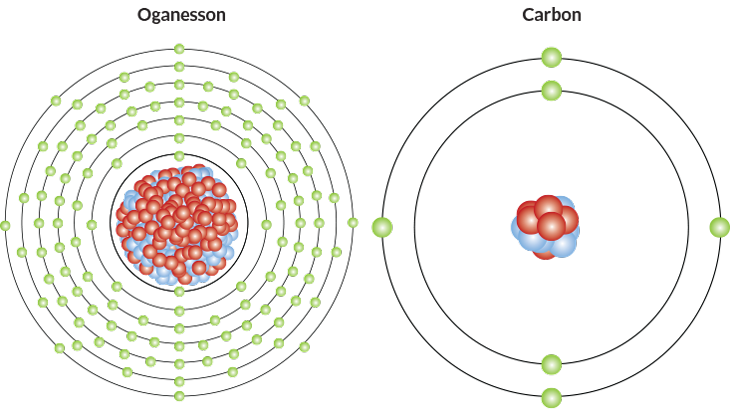
Para núcleos repletos de mais de 100 prótons, um tipo especial de física ocupa o centro do palco. Os elétrons giram em torno desses núcleos gigantes, às vezes ultrapassando 80% da velocidade da luz. De acordo com a teoria da relatividade especial de Einstein, quando as partículas se movem tão rapidamente, elas parecem ganhar massa. Essa propriedade altera a proximidade dos elétrons com o núcleo e, como resultado, a facilidade com que os átomos compartilham elétrons para produzir reações químicas. Nesses átomos, “as regras da relatividade e a sabedoria comum padrão entram em colapso”, diz o físico nuclear Witold Nazarewicz, da Universidade Estadual de Michigan, em East Lansing. “Temos que escrever novos livros sobre esses átomos.”
Alguns dos elementos mais familiares da tabela periódica já foram afetados pela relatividade especial. A teoria explica por que o ouro tem uma tonalidade amarelada e por que o mercúrio é líquido à temperatura ambiente ( SN: 18/02/17, p. 11 ). “Sem a relatividade, um carro não daria partida”, diz o químico teórico Pekka Pyykkö, da Universidade de Helsinque. As reações que alimentam a bateria de um carro dependem da relatividade especial.
A influência da relatividade pode aumentar à medida que os cientistas progridem ao longo da tabela periódica. Em 2018, em Physical Review Letters , Nazarewicz e colegas relataram que oganesson poderia ser totalmente bizarro ( SN Online: 12/02/18 ). O elemento mais pesado da mesa, oganesson, está entre os gases nobres reclusos que evitam reações com outros elementos. Mas oganesson contraria a tendência, sugerem os cálculos teóricos, e pode, em vez disso, ser reativo.
A química de Oganesson é um tema quente, mas os cientistas ainda não foram capazes de investigar diretamente suas propriedades com experimentos porque o oganesson é muito raro e passageiro. “Todos os teóricos estão agora a contornar este elemento tentando fazer previsões espectaculares”, diz a química teórica Valeria Pershina do GSI. Da mesma forma, alguns cálculos sugerem que o fleróvio pode inclinar-se na direção oposta, sendo relativamente inerte, embora habite a mesma coluna que elementos mais reativos, como o chumbo.
Os químicos estão se esforçando para testar esses cálculos sobre como os elementos superpesados se comportam. Mas não há nada de tradicional nessas experiências químicas. Não há cientistas de jaleco branco empunhando frascos e bicos de Bunsen. “Como fazemos essas coisas um átomo de cada vez, não podemos fazer o que a maioria das pessoas chama de química”, diz Shaughnessy, de Lawrence Livermore.
Os experimentos podem durar meses com apenas alguns átomos para mostrar isso. Os cientistas colocam esses átomos em contato com outros elementos para ver se os dois reagem. Na GSI, Düllmann e colegas estão analisando se o fleróvio adere às superfícies douradas. Da mesma forma, Shaughnessy e colegas estão testando se o fleróvio se fixará em moléculas em forma de anel, escolhidas de modo que o elemento pesado possa caber dentro do anel da molécula. Estes estudos irão testar a facilidade com que o fleróvio se liga a outros elementos, revelando se ele se comporta conforme o esperado com base na sua posição na tabela periódica.
Não são apenas as reações químicas que podem ficar malucas para elementos superpesados. Os núcleos atômicos podem ser deformados em vários formatos quando embalados com prótons. Oganesson pode ter uma “bolha” em seu núcleo , com menos prótons em seu centro do que em suas bordas ( SN: 26/11/16, p. 11 ). Núcleos ainda mais extremos podem ter formato de donut, diz Nazarewicz.
Mesmo as propriedades mais básicas destes elementos, como a sua massa, precisam de ser medidas. Embora os cientistas tenham estimado a massa dos vários isótopos dos novos elementos mais recentes usando medições indiretas, os argumentos que apoiam essas estimativas de massa não eram incontestáveis, diz Jacklyn Gates do Laboratório Nacional Lawrence Berkeley, na Califórnia. “Eles dependem da física e não de um obstáculo.”

Assim, Gates e colegas mediram diretamente as massas dos isótopos de niônio e moscóvio usando um acelerador em Lawrence Berkeley. Um aparelho chamado FIONA ajudou os pesquisadores a medir as massas, graças a campos eletromagnéticos que direcionavam um íon de cada elemento para um detector. O local onde cada íon atingiu indicava sua massa.
O isótopo de niônio que os pesquisadores detectaram tinha um número de massa de 284, o que significa que seu núcleo tinha um total combinado de 284 prótons e nêutrons. Moscovium tinha um número de massa de 288. Essas massas foram as previstas , relataram os cientistas em novembro na Physical Review Letters . Demorou cerca de um mês apenas para encontrar um átomo de cada elemento.
Vistas da ilha
Se os investigadores conseguissem persuadir estes elementos fugazes a viver mais tempo, estudar as suas propriedades poderia ser mais fácil. Os cientistas captaram visões atraentes de aumento da expectativa de vida fora de alcance – a lendária ilha da estabilidade ( SN: 05/06/10, p. 26 ). Os cientistas esperam que os isótopos daquela ilha, que estaria repleta de muitos neutrões, possam viver o suficiente para que a sua química possa ser estudada em detalhe.
Quando a ideia de uma ilha de estabilidade foi proposta na década de 1960, os cientistas sugeriram que os isótopos nas suas costas poderiam viver milhões de anos. Desde então, os avanços na física teórica derrubaram esse prazo, diz Nazarewicz. Em vez disso, os físicos nucleares esperam agora que os habitantes da ilha permaneçam por aqui durante minutos, horas ou talvez até um dia – uma eternidade agradável para elementos superpesados.
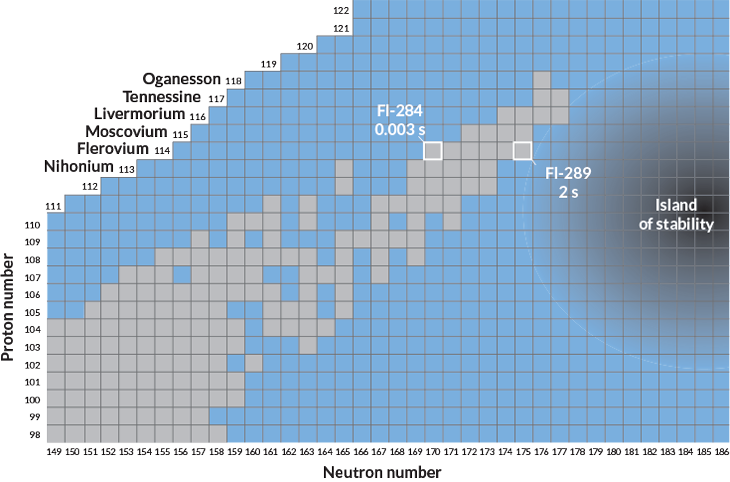
Para alcançar a ilha da estabilidade, os cientistas devem criar novos isótopos de elementos conhecidos. Os pesquisadores já sabem em que direção precisam remar: eles devem enfiar mais nêutrons nos núcleos dos elementos superpesados que já foram descobertos. Atualmente, os cientistas não conseguem produzir átomos com nêutrons suficientes para chegar ao centro da ilha, onde se espera que os isótopos sejam mais estáveis. Mas os sinais da existência desta ilha já são claros. As meias-vidas dos elementos superpesados tendem a aumentar à medida que os cientistas colocam mais nêutrons em cada núcleo, aproximando-se da ilha. A meia-vida do Fleróvio aumenta quase um fator de 700 à medida que mais cinco nêutrons são adicionados, de três milissegundos para dois segundos.
Chegar a esta ilha “é o nosso grande sonho”, diz Haba. “Infelizmente, não temos um método muito bom para chegar à ilha.” Acredita-se que essa ilha esteja centrada em torno de isótopos que possuem cerca de 184 nêutrons e algo em torno de 110 prótons. A produção de tais núcleos ricos em nêutrons exigiria técnicas novas e difíceis, como o uso de feixes de partículas radioativas em vez de estáveis. Embora os feixes radioativos possam ser produzidos em RIKEN, diz Haba, os feixes não são intensos o suficiente para produzir novos elementos a uma taxa razoável.
Ainda assim, detetives de elementos superpesados continuam tentando aprender como esses átomos estranhos se comportam.
Fim da linha
Para compreender plenamente os extremos da natureza, os cientistas querem saber onde termina a tabela periódica.
“Todo mundo sabe que em algum momento haverá um fim”, diz Düllmann. “Haverá um elemento mais pesado, em última análise.” A tabela estará concluída quando descobrirmos todos os elementos com isótopos que vivem pelo menos um centésimo de trilionésimo de segundo. Esse é o limite para o que se qualifica como elemento, de acordo com os padrões estabelecidos pela União Internacional de Química Pura e Aplicada. Núcleos mais efêmeros não teriam tempo suficiente para reunir um grupo de elétrons. Como a troca de elétrons é a base das reações químicas, núcleos isolados não exibiriam nenhuma química e, portanto, não merecem um lugar na mesa.
“É difícil dizer exatamente onde isso terminará”, diz Nazarewicz. Os cálculos sobre a rapidez com que um núcleo irá decair por fissão, ou divisão em dois, são incertos, o que torna difícil estimar quanto tempo os elementos poderão viver sem realmente os criar.

E a mesa final pode conter lacunas ou outras características estranhas. Isso poderia acontecer se, dentro de uma fileira de elementos, houvesse um ponto para o qual nenhum isótopo persistisse por tempo suficiente para ser qualificado como elemento.
Outra idiossincrasia: os elementos não podem ser organizados em ordem sequencial de acordo com o número de prótons que contêm , de acordo com cálculos em um artigo de 2011 de Pyykkö na Physical Chemistry Chemical Physics . O elemento 139, por exemplo, pode ficar à direita do elemento 164 – se tais elementos pesados realmente existirem. Isso ocorre porque a relatividade especial altera a ordem normal em que os elétrons se encaixam nas camadas, arranjos que definem como os elétrons giram em torno do átomo. Esse padrão de preenchimento da concha é o que dá forma à tabela periódica, e o preenchimento incomum pode significar que os cientistas decidam atribuir elementos a pontos fora de ordem.
Mas as adições à tabela podem secar antes que isso aconteça se os cientistas atingirem o limite da sua capacidade de criar elementos mais pesados. Quando os elementos vivem frações minúsculas de segundo, até mesmo a viagem do átomo até um detector pode demorar muito; o elemento decairia antes mesmo de ter a chance de ser localizado.
Na realidade, não há uma ideia clara de como procurar elementos além de 119 e 120. Mas o quadro já parecia sombrio antes.
“Não devemos subestimar a próxima geração. Eles podem ter ideias inteligentes. Eles terão novas tecnologias”, diz Düllmann. “O próximo elemento é sempre o mais difícil. Mas provavelmente não é o último.”